Récemment mis en lumière par une actualité tragique, les essais cliniques sont pourtant essentiels à la mise au point de nouveaux médicaments. Une recherche bibliographique portant sur une maladie ou un traitement peut nécessiter de cibler précisément ce type d’étude. Voici donc un petit tour d’horizon – non exhaustif – de ressources permettant de trouver des références d’essais cliniques, menés en France et dans le monde.
PubMed
La base de données Medline, produite par la NLM (National Library of Medicine, aux Etats-Unis) et accessible via l’interface PubMed, recense environ 26 millions de références d’articles, issus de plus de 5 600 revues médicales.
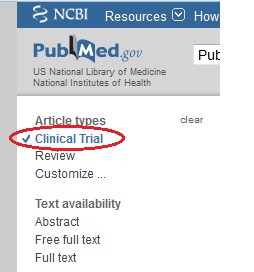
Lors de l’affichage des résultats, il est possible d’utiliser dans la colonne de gauche le filtre Article Types pour limiter la recherche aux essais cliniques : pour cela, il suffit de cocher Clinical Trial.
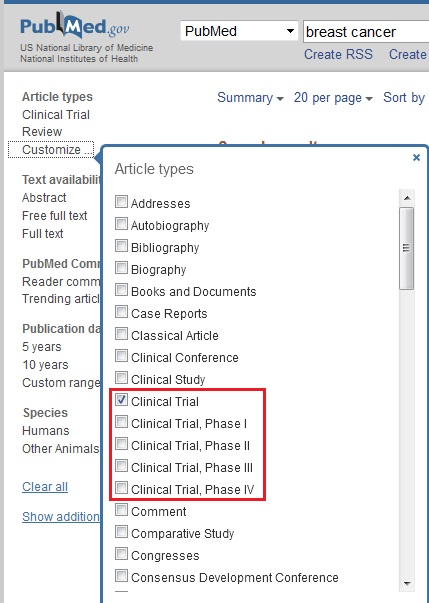
En cliquant sur Customize sous la liste proposée par défaut, on accède à la liste complète des types d’articles référencés dans PubMed : cela permet de sélectionner les essais cliniques de phase I, phase II, phase III, etc.
Attention, l’utilisation de PubMed est complexe et nécessite de maîtriser un langage contrôlé, le MeSH, dont l’utilisation est indispensable pour obtenir une liste de résultats courte et pertinente. Pour en savoir plus, vous pouvez assister à une formation gratuite à la BIU Santé, consulter notre tutoriel en ligne ou regarder les vidéos tutorielles DocToBib.
ClinicalTrials.gov
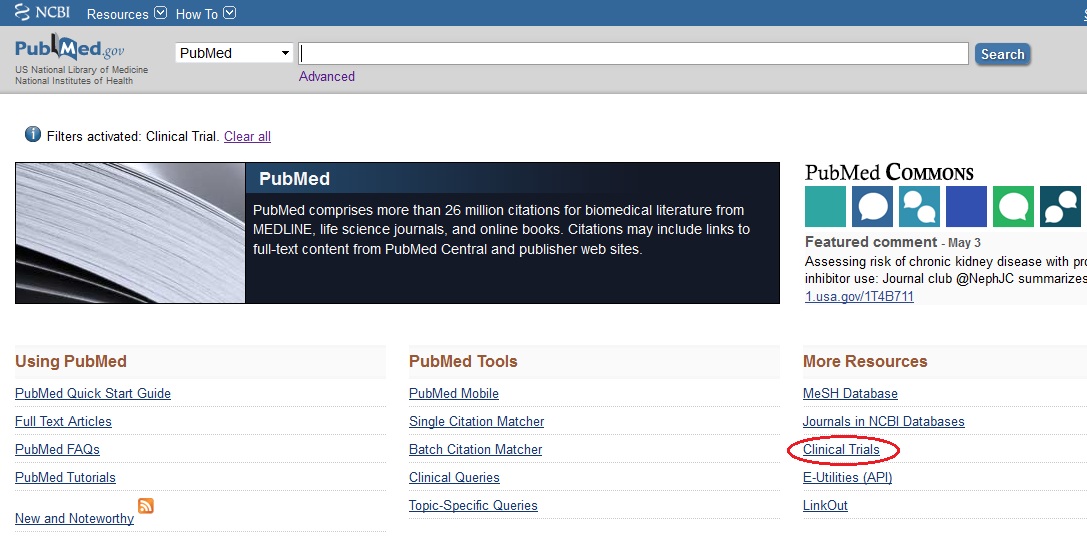
La base ClinicalTrials, produite par la NLM (comme PubMed), est accessible via la page d’accueil de PubMed ou directement à l’adresse https://clinicaltrials.gov/.
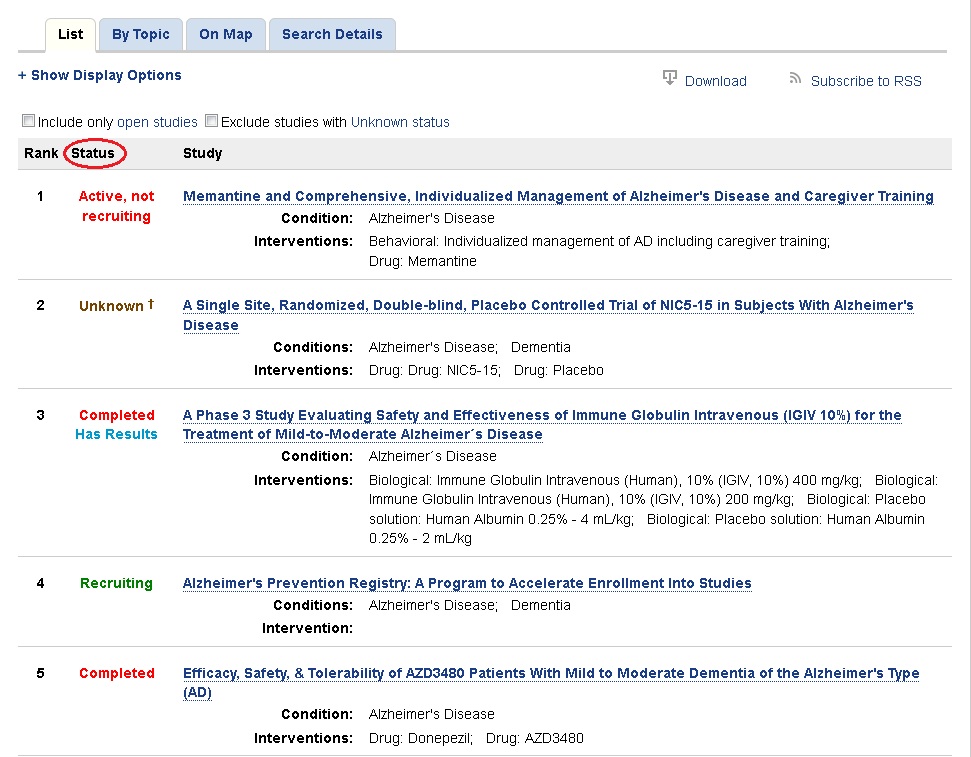
Cette base donne accès à plus de 200 000 essais cliniques du monde entier. Son intérêt est qu’elle recense des essais annoncés ou en cours, donc pas encore publiés dans des revues scientifiques et non encore indexés dans PubMed. Dans la liste des résultats, la colonne Status permet de distinguer les différentes étapes de l’essai : terminé (avec résultats disponibles), terminé (résultats en cours de traitement), en cours, non débuté (en attente d’inclusion), etc.
Un tri géographique des résultats est possible, via l’onglet On Map :
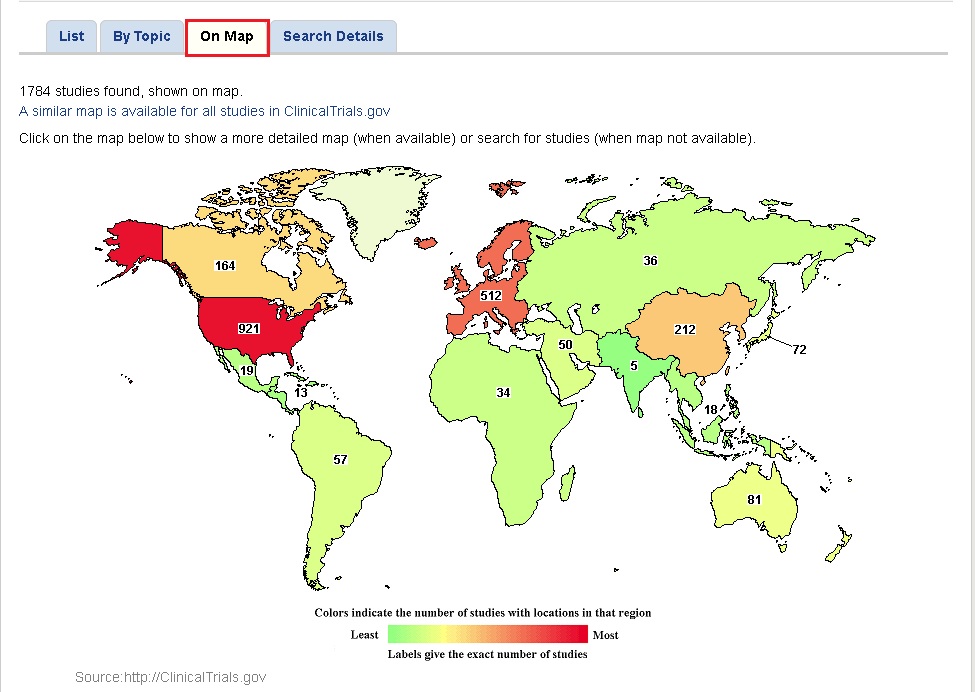
Il permet notamment d’isoler les essais cliniques menés en France (pour cela, cliquer sur l’Europe sur la carte du monde puis sur la France elle-même).
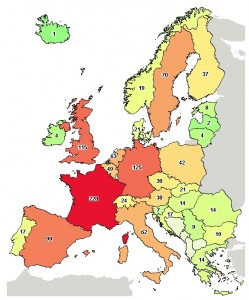
Pour mieux connaître le fonctionnement de ClinicalTrials, vous pouvez :
Répertoires français
En France, c’est l’ANSM (Agence nationale de sécurité du médicament et des produits de santé) qui autorise les essais cliniques et propose sur son site la consultation du Répertoire public des essais cliniques de médicaments menés en France (y compris les essais cliniques de thérapie cellulaire ou génique).
Le répertoire comprend les principales informations concernant l’essai : titre et numéro d’enregistrement européen, identité et coordonnées du promoteur, autres pays concernés (le cas échéant), brève description, objectifs et méthodologie de la recherche, ainsi que son état d’avancement.
Outre ce répertoire, il existe pour certaines pathologies des registres spécialisés, produits par d’autres institutions, en coordination avec l’ANSM :
Pour en savoir plus, consultez les pages dédiées aux essais cliniques sur le site de l’ANSM.
Répertoire européen
Le registre des essais cliniques de l’Agence européenne du médicament (EU clinical trials register) recense les essais cliniques menés dans l’Union européenne.
Mis en œuvre en 2004 conformément à la directive 2001/20/CE relative à l’application de bonnes pratiques dans la conduite d’essais cliniques de médicaments à usage humain, il est alimenté par les organismes responsables en matière d’essais cliniques des pays de l’Union.
il recense près de 28 000 essais cliniques, ainsi qu’environ 18 000 essais cliniques en pédiatrie.
Répertoire mondial
Un nouveau portail, OpenTrials, apparu en 2015, se donne pour objectif de recenser les essais cliniques du monde entier.
Pour en savoir plus, vous pouvez lire cet article (en anglais) paru dans BioMedCentral.
Benjamin Macé









 « Cette base de données comprend aujourd’hui plus de 800 000 références issues de PubMed mais aussi de 72 journaux scientifiques qui n’y figurent pas et de 53 qui y figurent de façon incomplète. Si l’on considère uniquement les années supérieures à 2000, la moitié du contenu de LiSSa est inédite. Plus de 80 000 résumés en français sont également proposés.
« Cette base de données comprend aujourd’hui plus de 800 000 références issues de PubMed mais aussi de 72 journaux scientifiques qui n’y figurent pas et de 53 qui y figurent de façon incomplète. Si l’on considère uniquement les années supérieures à 2000, la moitié du contenu de LiSSa est inédite. Plus de 80 000 résumés en français sont également proposés. Les formations sont gratuites et s’adressent aux lecteurs inscrits à la bibliothèque, ainsi qu’à tous les professionnels de santé et étudiants en médecine, odontologie et sciences paramédicales, à partir de la troisième année d’étude.
Les formations sont gratuites et s’adressent aux lecteurs inscrits à la bibliothèque, ainsi qu’à tous les professionnels de santé et étudiants en médecine, odontologie et sciences paramédicales, à partir de la troisième année d’étude.